Rachis | Pathologie intra-canalaire
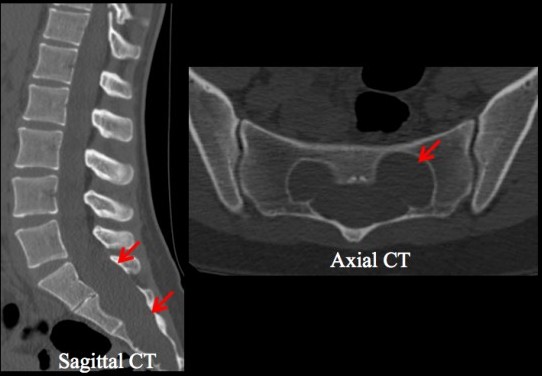
Douleur du pli inguinal gauche chez un homme de 53 ans avec TDM initial sans anomalie expliquant la symptomatologie clinique (TDM étage D12 L1, avec foramen G normal (étoile bleu))
Réalisation secondaire d’une IRM avec découverte d’une Masse unique au niveau épidural antéro latéral gauche D12 L1 (flèche rouge).
Les caractéristiques morphologiques, de signal et topographiques de cette lésion (isosignal en pondération T1, avec prise de contraste intense, localisation intra durale et extra médullaire) évoquent en premier lieu une tumeur primitive de type neurinome par argument de fréquence. En effet, la prise de contraste globale ainsi que l’aspect normal du disque en regard élimine une hernie exclue tandis que l’abscence de raccordement méningé élimine un méningiome. On ne retrouve cepandant pas d’elargissement en sablier du foramen correspondant.
En cas de neurinome multiple, une neurofibromatose doit être recherchée.
Pascual-Castroviejo I et al., Bilateral spinal neurofibromas in patients with neurofibromatosis 1, Brain Dev, 2012.
Histoire clinique
Jeune patiente de 20 ans adressée à l’IRM pour une lombosciatique droite rebelle au traitement médical bien conduit.
TDM déjà réalisée montrant une masse de densité liquidienne occupant la totalité du canal rachidien sacré avec important scalloping sacré (flèches rouges).
Interprétation de l’IRM
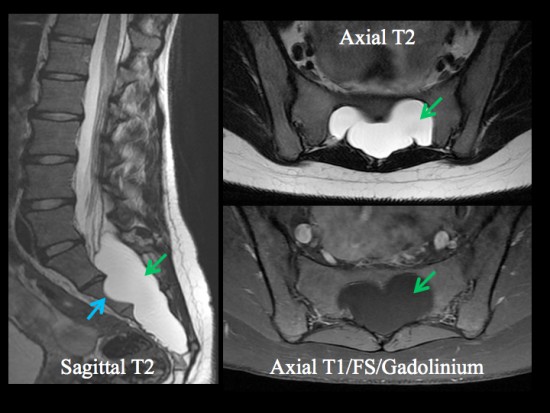
Le canal rachidien sacré est occupé en totalité par une masse kystique (hypersignal T2, hyposignal T1 sans rehaussement par le Gadolinium) non cloisonnée, à parois fines et sans aucun élément tissulaire et notamment nerveux (flèches vertes). Cette masse est de localisation extradurale et centrale au sein du canal.
Elle est expansive avec un important scalloping sur les pièces osseuses mais il n’y a aucun envahissement osseux ou des parties molles extra-canalaires (flèches bleues).
Il reste très difficile de mettre en évidence une éventuelle communication entre ce kyste et le sac dural.
Il n’y a pas d’autre anomalie significative.
Diagnostic
Méningocèle intra-sacrée occulte ou kyste méningé sacré ou kyste méningé de type 1B.
Physiopathologie et clinique
Il s’agit au départ d’un diverticule développé aux dépens de l’espace sous-arachnoïdien sacré, qui va ensuite former un véritable kyste extradural sous l’effet d’un mécanisme de « valve anti-reflux » qui permettra au LCR de rentrer dans le kyste mais ne pas en sortir. Sous l’effet de la pression du LCR, ce kyste entraine un remodelage avec érosion des pièces osseuses adjacentes, sans envahissement.
Il ne contient aucun élément nerveux et il n’y a pas de hernie des méninges. Il communique le plus souvent avec l’espace sous-arachnoïdien par un fin pédicule. Il est recouvert d’une membrane fibreuse et plus ou moins d’une simple couche interne de membrane arachnoïdienne.
Il peut être associé à des kystes de Tarlov, à un dysraphisme spinal postérieur ou à une moelle attachée.
Il représente 1 à 3% des tumeurs spinales. Sa prévalence est inconnue mais inférieure à celle des kystes de Tarlov.
Sa répartition est assez ubiquitaire et il est le plus souvent de découverte fortuite car asymptomatique ou à l’origine de douleur, de sciatalgie, de paresthésies périnéales et de dysfonction vésicale.
De façon plus rare, il est à l’origine de troubles digestifs (constipation, incontinence) et d’un syndrome de la moelle attachée. Ces signes cliniques peuvent être exacerbés lors des changements de position ou d’un Valsalva.
Imagerie
Le diagnostic repose sur l’IRM avec injection de Gadolinium qui permettra de faire le diagnostic positif, de rechercher les lésions associées (kystes de Tarlov, dysraphisme spinal postérieur, moelle attachée) et d’éliminer les diagnostics différentiels :
- Kystes de Tarlov : dilatation congénitale de la gaine méningée des racines nerveuses avec des kystes souvent multiples et excentrés,
- Méningocèle postérieure : protrusion au niveau des parties molles sous-cutanées via un dysraphisme postérieur,
- Dysplasie durale : le scalloping vertébral est étendu à l’étage lombaire.
Les séquences T1, T2 et T1 Fat Sat après injection de Gadolinium montreront un kyste simple intra-sacré de localisation extradurale centrale, sans élément tissulaire et sans hernie des méninges, dont la communication avec l’espace sous-arachnoïdien n’est pas toujours mise en évidence et entrainant généralement un important scalloping vertébral limité à l’étage sacré et sans envahissement des parties molles péri-rachidiennes.
Bibliographie
1-Ross JS and co. Diagnostic imaging: Spine. Amirsys, 2010.
2-Diel J and co. The sacrum: pathologic spectrum, multimodality imaging, and subspecialty approach. Radiographics. 21(1):83-104, 2001.
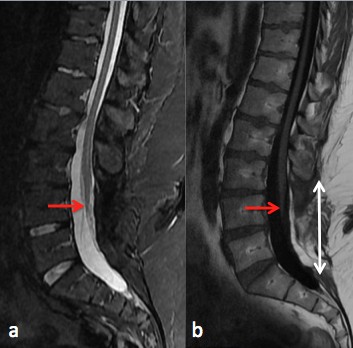
Fig 1: IRM du rachis lombaire en coupes sagittales STIR(a) et T1(b). Moelle basse attachée se terminant au niveau de L4 (flèche rouge). Défaut de fermeture de l’arcpostérieur de L3 à S2 (b, double flèche blanche).
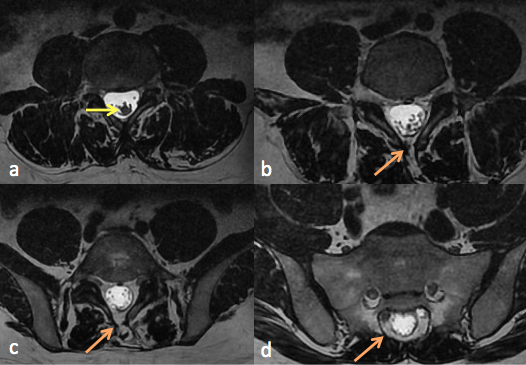
Fig 2: IRM du rachis lombaire en coupes axiales T2. Epaississement du filum terminale >2mm (a, flèchejaune). Défaut de fermeture de l’arcpostérieur (flèche orange) en L4 (b) L5 (c) et S2 (d).
Conclusion: Moëlle attachée basse en L4 secondaireà un épaississement du filum terminale avec défaut de fermeture de l’arcpostérieur chez un adulte.
Ref: - Tethered cord syndrome in adults.Klekamp J. J NeurosurgSpine. 2011 Sep; 15(3):258-70. Epub 2011 May 20.
-The tethered cord syndrome in adults with spina bifida occulta. Lapsiwala SB, Iskandar BJ (2004) Neurol Res 26:735–740
Homme de 70ans. Sciatalgie L5 gauche hyperalgique.
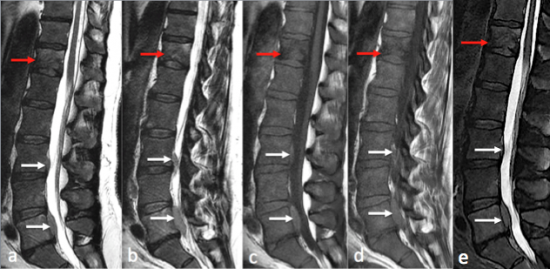
Fig1: IRM du rachis lombaire en coupes sagittales T2 (a,b) et T1 (c,d) et STIR (e).
Masses tissulaires épidurales antérieures en L3 et L5 en discret hypersignal T2 et T1 (flèches blanches). Présence d'une lésion osseuse suspecte du corps vertébral de T12 en franc hyposignal T1 (flèches rouges) et hypersignal STIR (e, flèche rouge).
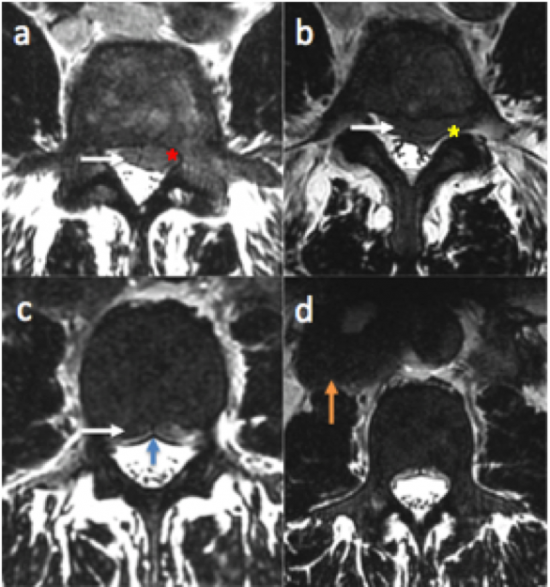
Fig 2: IRM du rachis lombaire, séquences axiales T2. Masse épidurale antérieure lombaire (flèches blanches) à l'étage L4-L5 ,responsable d'une compression de la racine L5 gauche au niveau du récessus latéral (a, étoile rouge) et au niveau foraminal gauche en L5-S1 (b, étoile jaune). Cette compression est responsable de la symptomatologie du patient.
A noter l'aspect en "ambroise de rideau" témoignant d'une localisation épidurale des masses (c, flèche bleue).
Multiples adénomégalies rétropéritonéales (d, flèche orange).
Conclusion:
L'atteinte à la fois épidurale, vertébrale et rétropéritonéale est en faveur d'une hémopathie maligne de type lymphome.
La TEP-TDM retrouve également une atteinte splénique, ganglionnaire sus et sous-diaphragmatique et osseuse au niveau de l'ischion gauche.
Les biopsies ganglionnaires rétropéritonéales ont été réalisées et l'analyse histologique révèle un lymphome B folliculaire de grade 1-2.
Le lymphome épidural est une entité rare, consituant environ 10% des tumeurs épidurales.
0.1 à 3.3% des lymphomes non hodgkiniens présentent une atteinte épidurale.
L'atteinte épidurale peut être d'origine hématogène ou secondaire à une atteinte osseuse vertébrale de proximité.
Une discrète prédominance masculine est rapportée.
Ref: Boukobza M, Mazel C, Touboul E. Primary spinal and spinal epidural non-Hodgkin’s lymphoma with spinal cord compression. Neuroradiology. 1996;38:333–7. doi: 10.1007/BF00596582.
Patient de 20 ans présentant une atrophie des loges musculaires des avant bras, avec un EMG retrouvant une atteinte de C7 à T1 ; Exploration par IRM cervicale dynamique, en position neutre et en flexion cervicale.
Coupes sagittales pondérées T2 explorant le rachis et la moelle cervicales :
Image (a) : Acquisition en position neutre : absence de réduction de calibre du canal cervical ou de signe de compression médullaire. On notera un amincissement du calibre de la moelle cervicale à hauteur de C5-C6.
Image (b) Acquisition en flexion cervicale : l'examen décele un déplacement antérieur de la moelle cervicale et du sac dural à hauteur de C5-C6, à l'origine d'un aspect aplati. Il s'y associe un décollement épidural postérieur (flèches oranges). Il n'y a pas d'anomalie de signal médullaire.
Coupes axiales pondérées T2 explorant le rachis et la moelle cervicales :
Image (c) : Acquisition en position neutre : le canal cervical et les foramens sont libres, sans anomalie de signal médullaire.
Image (d) Acquisition en flexion cervicale : l'examen décele un déplacement antérieur de la moelle cervicale et du sac dural à hauteur de C5-C6. Il s'y associe un décollement épidural postérieur (flèches oranges). Il n'y a pas d'anomalie de signal médullaire.
Ce cas illustre une maladie de Hirayama ou amyotrophie juvénile distale du membre supérieur.
La maladie d’Hirayama est une myélopathie cervicale basse rare atteignant les adultes jeunes. Elle est responsable d’une atteinte motrice pure distale des membres supérieurs, d’évolution lentement progressive dans le territoire des métamères C7 à T1. Elle serait provoquée par les mouvements de flexion du cou. L’imagerie par résonance magnétique (IRM) en position neutre recherche une anomalie de courbure cervicale, une atrophie avec aplatissement de la moelle cervicale, un hypersignal médullaire antérieur et surtout un défaut d’accolement postérieur du sac dural. En cas de suspicion diagnostique, une IRM en flexion doit être réalisée pour mettre en évidence un déplacement antérieur de la moelle et du sac dural, un élargissement de l’espace épidural postérieur, une majoration de l’aplatissement médullaire et une congestion des veines épidurales.
L’électromyogramme (EMG) retrouve une atteinte neurogène des territoires C7-C8-T1.
L’hypothèse physiopathologique actuelle repose sur une atteinte ischémique chronique de la moelle cervicale basse provoquée par l’écrasement médullaire contre le corps vertébral, notamment lors des mouvements de flexion cervicale. (croissance disproportionnée entre le rachis et le sac dural)
Remerciements au Dr Marwan El Kadri pour ce cas clinique.
Références :
M. Dejobert, A. Geffray, C. Delpierre, B. Chassande, E. Larrieu, C. Magni La maladie d’Hirayama : à propos de trois cas
Hirayama K., Toyokura Y., Tsubaki T. Juvenile muscular atrophy of unilateral upper extremit: a new clinical entity Psychiatr Neurol Jpn 1959 ; 61 : 2190-2197
Hirayama K. Juvenile muscular atrophy localized in hands ans forearm: observation in 38 cases Rinsho Shinkkeigaku 1972 ; 12 : 313-324



